후천적 유전자 발현 조절과정 규명
국제학술지 ‘핵산 연구’에도 게재돼
전남대 김정선·이영철 교수팀
후천적 유전자 발현 변이에 의한 암을 치료할 신약 개발에 한걸음 다가갔다.
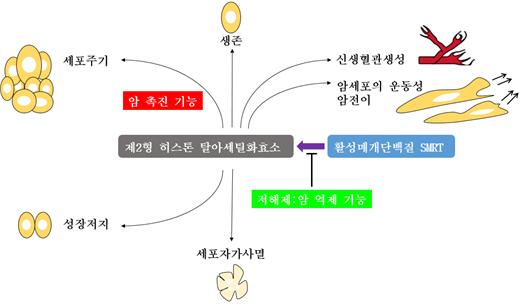
전남대 김정선‧이영철 교수 연구팀이 제2형 히스톤 탈아세틸화 효소의 활성이 제어되면서 후천적인 유전자 발현이 조절되는 분자생물학적 과정을 규명했다.

연구성과는 생화학 및 분자생물학분야 국제학술지인 ‘핵산 연구(Nucleic Acids Research)’ 10월 13일자에 게재됐다.
이 연구는 후천적 유전자 발현 변이에 의해 촉발되는 암, 종양혈관 형성억제, 면역조절, 심근비대증 등과 같은 질병을 치료 할 수 있는 새로운 신약 후보물질 개발에 필요한 이론적 토대를 마련한 것으로 평가되고 있다.
연구팀에 따르면 히스톤 및 비히스톤 단백질의 아세틸화에 의해 유전자 발현이 조절되는데, 아세틸화 패턴의 불균형이 다양한 암 생성과 밀접하게 관련된 것으로 알려져 있다.
이와 관련, 연구팀은 SMRT/NCoR의 RD3 도메인 내에 보존된 글라이신-세린-아이소루신 아미노산 서열을 포함하는 2개의 GSI 모티프가 탈아세틸화효소 4와의 결합에 중요하다는 것을 발견하였다. 또한 히스톤탈아세틸화효소 4와 펩타이드 복합체를 단백질 결정학 방법을 이용하여 이들 사이의 결합모형을 분자적 수준에서 시각화하고 돌연변이체 연구를 통하여 확인하였다.
김정선 교수는 “이 연구는 히스톤 아세틸화 관련 저해제의 부작용을 줄일 수 있는, 특이성 높은 저해제 개발에 활용될 것”이라며, “앞으로 이어질 후속 연구에서 개발되는 저해 물질이 제2형 탈아세틸화 효소 관련 질병 치료제의 신약이 될 것으로 기대된다.”고 말했다.
한편, 이 연구는 한국연구재단의 기초연구사업과 기초연구실사업(박희세)의 지원으로 이뤄졌으며, 박석열 박사(포항가속기연구소), 김광식 박사(생명과학기술학부), 황효정(화학과), 남택현(생명과학기술학부) 등 전남대 출신들이 연구원으로 참여했다.

